Bộ Y tế ‘chỉ mặt’ 3 nhóm thuốc giả đang len lỏi ngay trong nhà thuốc
Ba nhóm sản phẩm vừa bị Bộ Y tế “tuýt còi” là thuốc nhỏ mắt (Tobrex, Maxitrol, TobraDex), thuốc ngủ Lexomil liều cao và thuốc điều trị loãng xương Aclasta.
Bộ Y tế vừa ra loạt cảnh báo khẩn sau khi Cục Quản lý Dược tiếp nhận thông tin nhiều trường hợp thuốc và mỹ phẩm lưu hành có dấu hiệu không đúng quy định, thậm chí bị nghi là hàng giả.
Về thuốc ngủ Lexomil 6 mg, Cục cảnh báo lô thuốc mang số F3193F01, hạn dùng 12/2027, đã bị Công an TP.HCM thu giữ và được nhà sản xuất xác định là hàng giả. Sản phẩm này vốn là hàng được sản xuất cho thị trường Pháp và không được nhập khẩu chính ngạch vào Việt Nam. Cục nhấn mạnh Lexomil 6 mg hiện chưa có số đăng ký lưu hành tại Việt Nam, do đó việc xuất hiện trên thị trường là trái quy định và cần được rà soát, truy xuất nguồn gốc.
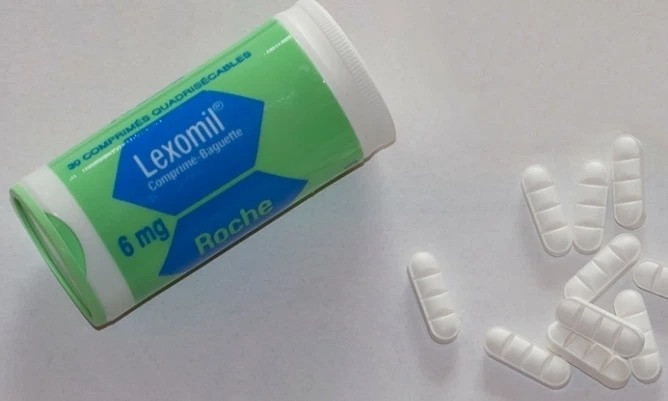 |
| Lô thuốc Lexomil 6 mg mang số F3193F01 được xác định là hàng giả. Ảnh minh họa |
Về Aclasta (chứa acid zoledronic), một nhà thuốc tại Kiên Giang phản ánh về lô thuốc có ngày sản xuất tháng 8/2024, hạn dùng đến 7/2027. Nhà đăng ký lưu hành khẳng định lô này không được sản xuất tại cơ sở chính thức và không được nhập khẩu theo đường chính ngạch. Kể từ tháng 5/2024, các lô Aclasta chính hãng đã sử dụng logo Sandoz thay cho logo Novartis. Những chai, hộp in logo cũ trong lô sản xuất sau mốc này bị nghi ngờ là giả. Cục Quản lý Dược yêu cầu cơ quan địa phương thu thập, xác minh và xử lý theo quy định.
 |
| Lô thuốc Aclasta có ngày sản xuất tháng 8/2024, hạn dùng đến 7/2027 cũng bị nghi hàng giả. Ảnh minh họa |
Nhóm thuốc nhỏ mắt cũng ghi nhận nhiều phản ánh. Novartis Việt Nam báo cáo bốn trường hợp, trong đó lô Tobrex 5 ml số VEE90A đã được xác minh là giả, 3 lô khác (Tobrex VEE98C, Maxitrol VFD09A và TobraDex VHN07A) được xếp vào danh sách nghi ngờ. Các sản phẩm bị báo cáo đều được phát hiện lưu hành ngoài hệ thống phân phối chính thức của nhà sản xuất, làm tăng rủi ro cho người sử dụng khi mua phải thuốc không rõ nguồn gốc.
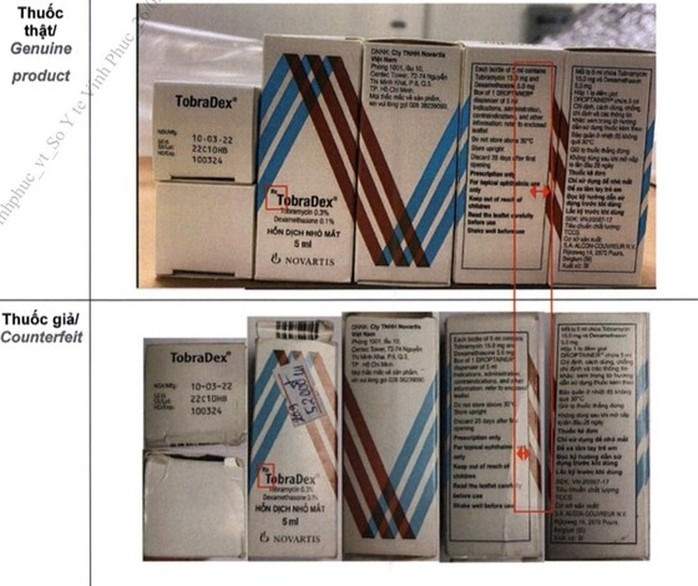 |
| Thuốc nhỏ mắt cũng bị nghi ngờ. Ảnh minh họa |
Thanh tra chuyên ngành còn phát hiện nhiều mỹ phẩm có công thức khác so với hồ sơ công bố. Cục Quản lý Dược đã yêu cầu Công ty TNHH Sản xuất và Thương mại Mỹ phẩm Đăng Dương thu hồi 5 dòng sản phẩm (các kem dưỡng/kem ngừa nám) và tiêu hủy theo quy định, đồng thời báo cáo kết quả thu hồi trước ngày 15/9. Trường hợp Công ty Gamma liên quan đến sản phẩm sữa rửa mặt Vinatid bị đình chỉ lưu hành, thu hồi và yêu cầu báo cáo kết quả trước ngày 30/9/2025.
Cục Quản lý Dược đã đề nghị Sở Y tế các tỉnh, thành phối hợp với cơ quan công an, nhà phân phối và các đơn vị liên quan khẩn trương truy xuất nguồn gốc, kiểm soát lưu thông các lô hàng nghi vấn và thông báo rộng rãi đến bệnh viện, nhà thuốc, hộ kinh doanh và người dân. Đồng thời, Cục khuyến cáo người dân chỉ mua thuốc, sản phẩm y tế tại cơ sở kinh doanh hợp pháp; không sử dụng thuốc, sản phẩm có nguồn gốc mập mờ hoặc lưu hành ngoài hệ thống phân phối chính thức. Các doanh nghiệp như DKSH, Sandoz, Novartis… được yêu cầu chủ động cung cấp thông tin, phối hợp trong công tác truy xuất.























